Mendelejevi tabel: Keemiliste elementide perioodilisussüsteem
Keemiliste elementide perioodilisustabel on süsteem, mis koondab kõik teadaolevad elemendid nende aatomnumbri, elektronkonfiguratsiooni ja korduvate keemiliste omaduste põhjal. See on asendamatu tööriist nii keemikutele, õpilastele kui ka teadlastele, aidates mõista elementide vahelisi seoseid ja ennustada nende käitumist.
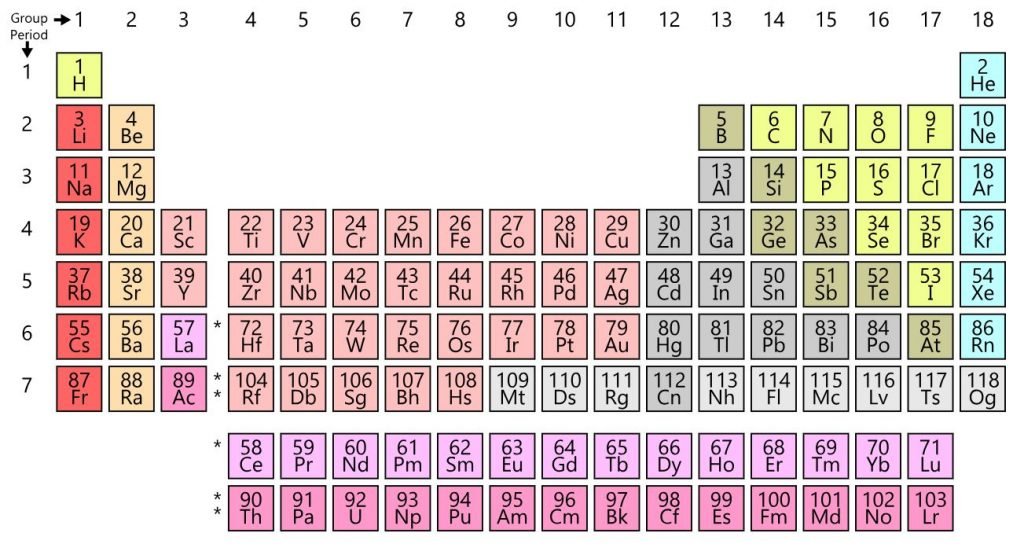
Kuidas perioodilisustabelit lugeda?
- Perioodid: Horisontaalsed read tabelis. Need näitavad elektronkihtide arvu aatomis.
- Rühmad: Vertikaalsed veerud. Sama rühma elementidel on sarnased keemilised omadused (nt leelismetallid või väärisgaasid).
- Aatomnumber: Näitab prootonite arvu aatomi tuumas ja määrab elemendi koha tabelis.
Keemiliste elementide loend
Elemendi otsing
| Nr | Sümbol | Element | Rühm / Kategooria |
|---|---|---|---|
| 1 | H | Vesinik | Mittemetall |
| 2 | He | Heelium | Väärisgaas |
| 3 | Li | Liitium | Leelismetall |
| 4 | Be | Berüllium | Leelismuldmetall |
| 5 | B | Boor | Poolmetall |
| 6 | C | Süsinik | Mittemetall |
| 7 | N | Lämmastik | Mittemetall |
| 8 | O | Hapnik | Mittemetall |
| 9 | F | Fluor | Halogeen |
| 10 | Ne | Neoon | Väärisgaas |
| 11 | Na | Naatrium | Leelismetall |
| 12 | Mg | Magneesium | Leelismuldmetall |
| 13 | Al | Alumiinium | Metall |
| 14 | Si | Ränisüsteem | Poolmetall |
| 15 | P | Fosfor | Mittemetall |
| 16 | S | Väävel | Mittemetall |
| 17 | Cl | Kloor | Halogeen |
| 18 | Ar | Argoon | Väärisgaas |
| 19 | K | Kaalium | Leelismetall |
| 20 | Ca | Kaltsium | Leelismuldmetall |
| 21 | Sc | Skandium | Siirdemetall |
| 22 | Ti | Titaan | Siirdemetall |
| 23 | V | Vanaadium | Siirdemetall |
| 24 | Cr | Kroom | Siirdemetall |
| 25 | Mn | Mangaan | Siirdemetall |
| 26 | Fe | Raud | Siirdemetall |
| 27 | Co | Koobalt | Siirdemetall |
| 28 | Ni | Nikkel | Siirdemetall |
| 29 | Cu | Vask | Siirdemetall |
| 30 | Zn | Tsink | Siirdemetall |
| 31 | Ga | Gallium | Metall |
| 32 | Ge | Germaanium | Poolmetall |
| 33 | As | Arseen | Poolmetall |
| 34 | Se | Seleen | Mittemetall |
| 35 | Br | Broom | Halogeen |
| 36 | Kr | Krüptoon | Väärisgaas |
| 37 | Rb | Rubiidium | Leelismetall |
| 38 | Sr | Strontsium | Leelismuldmetall |
| 39 | Y | Üttrium | Siirdemetall |
| 40 | Zr | Tsirkoonium | Siirdemetall |
| 41 | Nb | Nioobium | Siirdemetall |
| 42 | Mo | Molübdeen | Siirdemetall |
| 43 | Tc | Tehineetsium | Siirdemetall |
| 44 | Ru | Ruteenium | Siirdemetall |
| 45 | Rh | Roodium | Siirdemetall |
| 46 | Pd | Pallaadium | Siirdemetall |
| 47 | Ag | Hõbe | Siirdemetall |
| 48 | Cd | Kaadmium | Siirdemetall |
| 49 | In | Indium | Metall |
| 50 | Sn | Tina | Metall |
| 51 | Sb | Antimon | Poolmetall |
| 52 | Te | Telluur | Poolmetall |
| 53 | I | Jood | Halogeen |
| 54 | Xe | Ksenoon | Väärisgaas |
| 55 | Cs | Tseesium | Leelismetall |
| 56 | Ba | Baarium | Leelismuldmetall |
| 57 | La | Lantaan | Lantanoid |
| 58 | Ce | Tseerium | Lantanoid |
| 59 | Pr | Praseodüüm | Lantanoid |
| 60 | Nd | Neodüüm | Lantanoid |
| 61 | Pm | Promeetium | Lantanoid |
| 62 | Sm | Samaarium | Lantanoid |
| 63 | Eu | Euroopium | Lantanoid |
| 64 | Gd | Gadoliinium | Lantanoid |
| 65 | Tb | Terbium | Lantanoid |
| 66 | Dy | Düsproosium | Lantanoid |
| 67 | Ho | Holmium | Lantanoid |
| 68 | Er | Erbium | Lantanoid |
| 69 | Tm | Tuulium | Lantanoid |
| 70 | Yb | Ütterbium | Lantanoid |
| 71 | Lu | Luteetsium | Lantanoid |
| 72 | Hf | Hafnium | Siirdemetall |
| 73 | Ta | Tantaal | Siirdemetall |
| 74 | W | Volfram | Siirdemetall |
| 75 | Re | Reenium | Siirdemetall |
| 76 | Os | Osmium | Siirdemetall |
| 77 | Ir | Iriidium | Siirdemetall |
| 78 | Pt | Plaatina | Siirdemetall |
| 79 | Au | Kuld | Siirdemetall |
| 80 | Hg | Elavhõbe | Siirdemetall |
| 81 | Tl | Tallium | Metall |
| 82 | Pb | Plii | Metall |
| 83 | Bi | Vismut | Metall |
| 84 | Po | Poloonium | Poolmetall |
| 85 | At | Astaat | Poolmetall |
| 86 | Rn | Radoon | Väärisgaas |
| 87 | Fr | Frantsium | Leelismetall |
| 88 | Ra | Raadium | Leelismuldmetall |
| 89 | Ac | Aktinium | Aktinoid |
| 90 | Th | Toorium | Aktinoid |
| 91 | Pa | Protaktiinium | Aktinoid |
| 92 | U | Uraan | Aktinoid |
| 93 | Np | Neptuunium | Aktinoid |
| 94 | Pu | Plutoonium | Aktinoid |
| 95 | Am | Ameriitsium | Aktinoid |
| 96 | Cm | Kuurium | Aktinoid |
| 97 | Bk | Berkeelium | Aktinoid |
| 98 | Cf | Kalifornium | Aktinoid |
| 99 | Es | Einsteinium | Aktinoid |
| 100 | Fm | Fermium | Aktinoid |
| 101 | Md | Mendeleevium | Aktinoid |
| 102 | No | Nobelium | Aktinoid |
| 103 | Lr | Lourensium | Aktinoid |
| 104 | Rf | Rutherfordium | Siirdemetall |
| 105 | Db | Dubnium | Siirdemetall |
| 106 | Sg | Seaborgium | Siirdemetall |
| 107 | Bh | Bohrium | Siirdemetall |
| 108 | Hs | Hassium | Siirdemetall |
| 109 | Mt | Meitneerium | Siirdemetall |
| 110 | Ds | Darmstadtium | Siirdemetall |
| 111 | Rg | Röntgeenium | Siirdemetall |
| 112 | Cn | Koperniitsium | Siirdemetall |
| 113 | Nh | Nihhoonium | Metall |
| 114 | Fl | Fleroovium | Metall |
| 115 | Mc | Moskoovium | Metall |
| 116 | Lv | Livermoorium | Metall |
| 117 | Ts | Tennessiin | Halogeen |
| 118 | Og | Oganessoon | Väärisgaas |
Keemiliste elementide rühmad ja omadused
- Leelismetallid: Väga reaktsioonivõimelised metallid (nt Liitium, Naatrium).
- Väärisgaasid: Lõhnatud, värvitud ja väga madala reaktsioonivõimega elemendid (nt Heelium, Neoon).
- Halogeenid: Mittemetallid, mis moodustavad sooli (nt Fluor, Kloor).
- Siirdemetallid: Tugevad ja hea elektrijuhtivusega metallid (nt Raud, Kuld).
- Lantanoidid ja aktinoidid: Tuntud ka kui haruldased muldmetallid, paljud neist on radioaktiivsed.
Korduma kippuvad küsimused Mendelejevi tabeli kohta
Kes leiutas perioodilisustabeli?
Esimese laialdaselt tunnustatud tabeli koostas Vene keemik Dmitri Mendelejev 1869. aastal. Ta jättis tabelisse tühjad kohad veel avastamata elementide jaoks.
Mitu elementi on tabelis?
Praeguse seisuga on perioodilisustabelis 118 kinnitatud elementi. Viimased neli (nihhoonium, moskoovium, tennessiin ja oganessoon) lisati ametlikult 2016. aastal.
Mis on kõige kergem element?
Kõige kergem element on vesinik (H), mille aatomnumber on 1 ja mis koosneb vaid ühest prootonist ja ühest elektronist.
Mis on kõige haruldasem element?
Looduslikult esinevatest elementidest peetakse üheks haruldasemaks astaati (At), mida leidub maakoores korraga vaid väga väikeses koguses.
Kuidas elemente tabelis järjestatakse?
Elemente järjestatakse aatomnumbri (prootonite arvu) suurenevas järjekorras, rühmitades neid sarnaste keemiliste omaduste põhjal.